文獻解讀
文獻解讀|Cell Research 系統代謝組學開拓三陰性乳腺癌精準治療新視角
新陳代謝重編碼是癌癥的一個標志。然而,目前仍然缺乏對三陰性乳腺癌(TNBC)代謝物的系統描述。本篇文章研究分析了330個TNBC樣本和149對正常乳腺組織的代謝組和脂質組,構建了完整的TNBC代謝組圖譜。結合之前建立的同一隊列的轉錄組和基因組,作者進行了TNBC代謝組和基因組學的綜合分析。該研究將TNBC分為三個不同的代謝組學亞型:C1,以富含神經酰胺和脂肪酸為特征;C2,氧化反應和糖基轉移相關代謝產物表達上調;C3,最低的代謝水平失調。基于這個新開發的代謝組數據集,作者對之前的TNBC轉錄組亞型進行了提煉,并確定了一些關鍵的亞型特異性代謝物以作為潛在的治療靶點。轉錄組雄激素受體(LAR)亞型與代謝組C1亞型重疊。對患者來源的類器官和異種移植模型的實驗表明,針對神經酰胺途徑的中間體鞘氨醇-1-磷酸(S1P),是一種很有前途的治療LAR腫瘤的方法。此外,轉錄組基礎細胞樣免疫抑制(BLIS)亞型包含兩個預后代謝組亞群(C2和C3),可以通過機器學習方法進行區分。作者發現n -乙酰天冬氨酸是一種重要的促腫瘤代謝物,也是高危BLIS腫瘤的潛在治療靶點。總之,該研究揭示了TNBC代謝組學的臨床意義,不僅可以優化轉錄組分型系統,還可以提出新的治療靶點。本代謝組學數據集可作為促進TNBC精準治療的有用公共資源。
該論文于2022年2月1日,由復旦大學附屬腫瘤醫院乳腺外科邵志敏教授、江一舟教授領銜團隊在 Cell Research(IF25.617)期刊發表,其題目為Comprehensive metabolomics expands precision medicine for triple-negative breast cancer 。

研究材料
330個TNBC樣本和149個匹配的正常組織樣本
技術方法
代謝組學,轉錄組學等
研究結果
TNBC的代謝組學和脂質組學分析
該研究表明,TNBC可分為三個代謝基因亞型,且對脂質代謝和糖酵解具有明顯的依賴性。作者對330個TNBC樣本的代謝組和脂質組進行了分析,以揭示代謝物整體變化規律。作者還將代謝組學與先前建立的基因組和轉錄組數據相結合,以探索TNBC的潛在代謝靶點,特別是轉錄組學的BLIS和LAR腫瘤。作者總共注釋了594個代謝物以及1944個脂質分子。同時在330個樣本中,作者得到了其中的258個樣本的轉錄組數據。這些共同構成了一個巨大的TNBC的數據集。
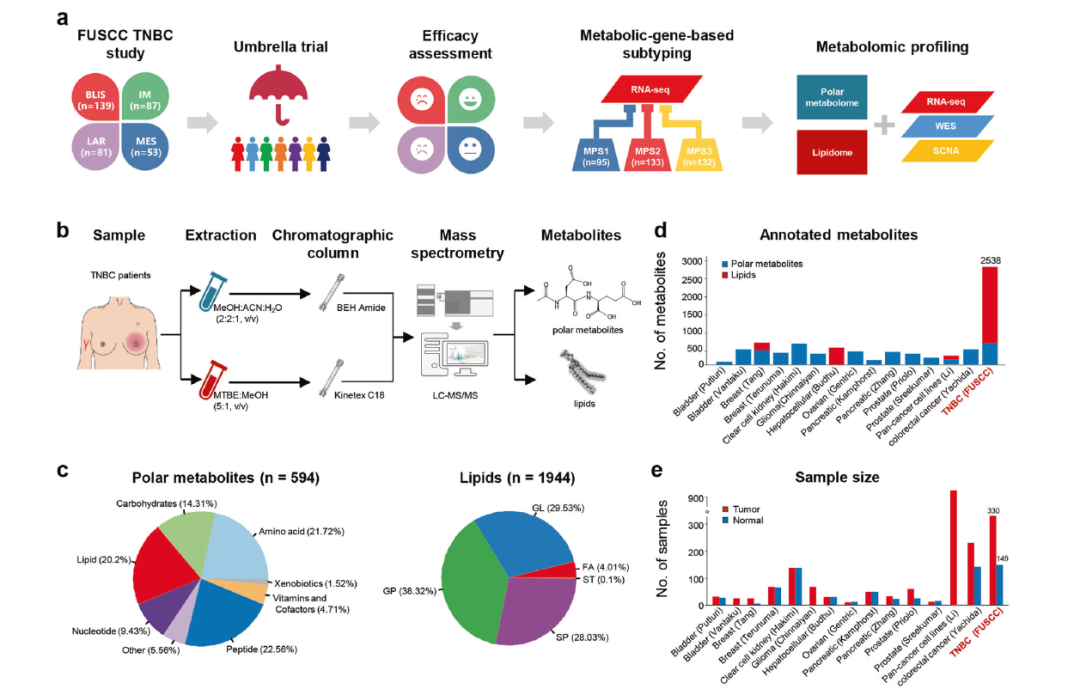
TNBC的代謝組學圖譜
作者對三陰性乳腺癌的代謝組學進行了研究。通過火山圖描述了594個注釋過的代謝物和1944個脂質。并且對不同種類的代謝物分別進行分類編碼。通過從代謝組學層面將TNBC分為三個不同的代謝亞組:C1,以神經酰胺和脂肪酸的富集為特征;C2,具有與氧化反應和糖基轉移相關的代謝產物的上調;而C3則是代謝失調程度最低的。
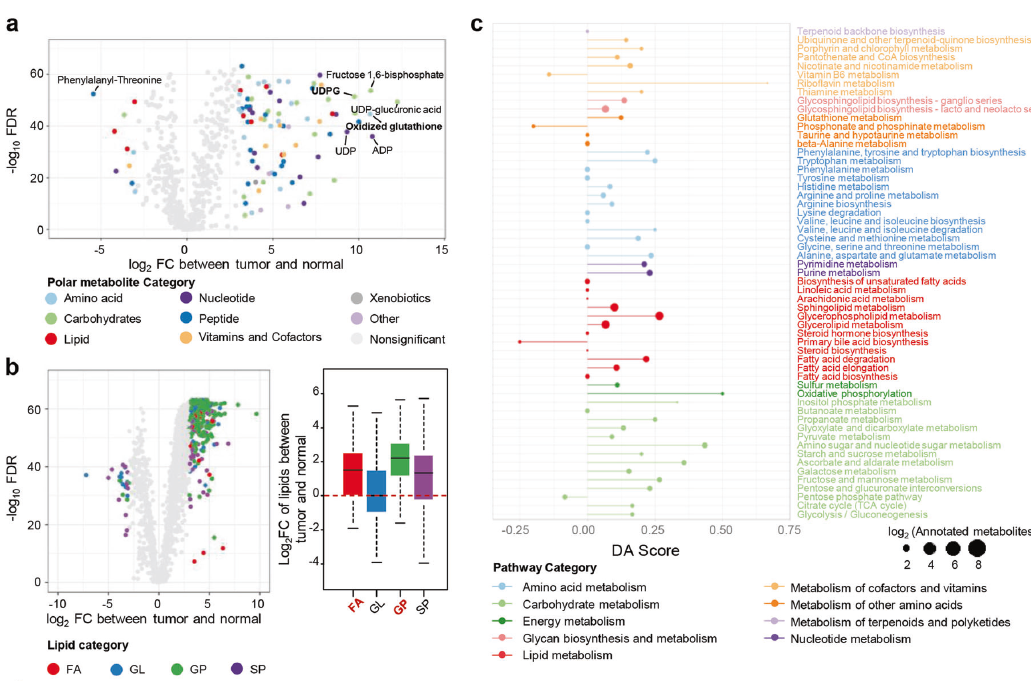
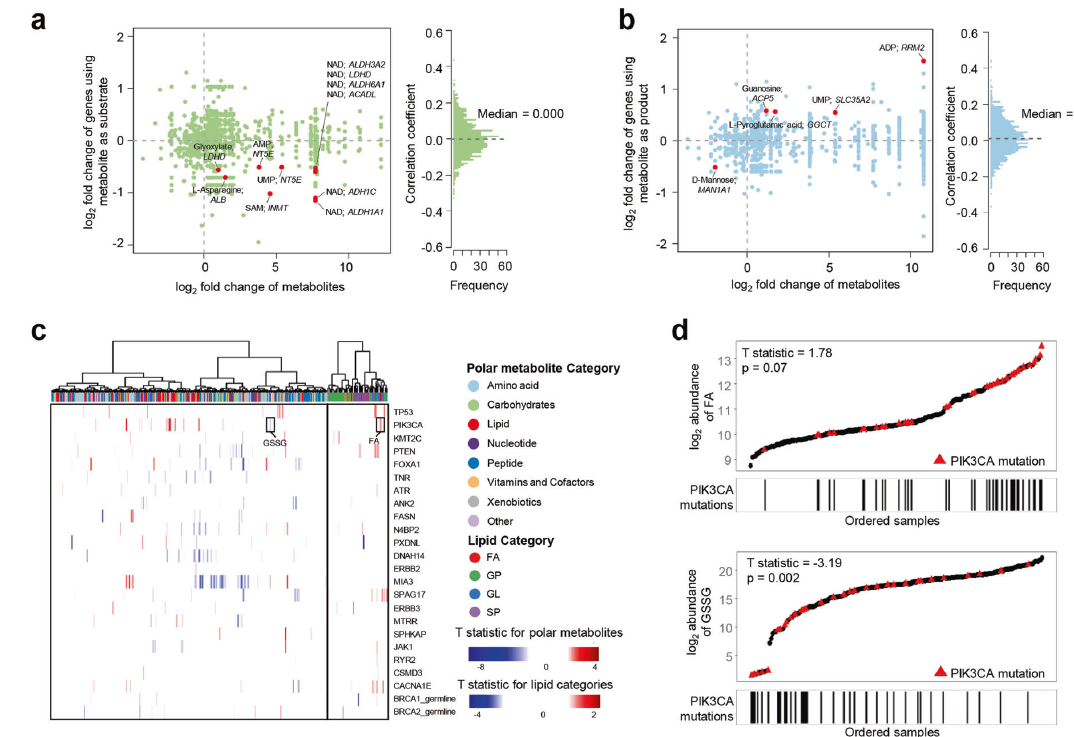
聯系多組學特征進行綜合分析
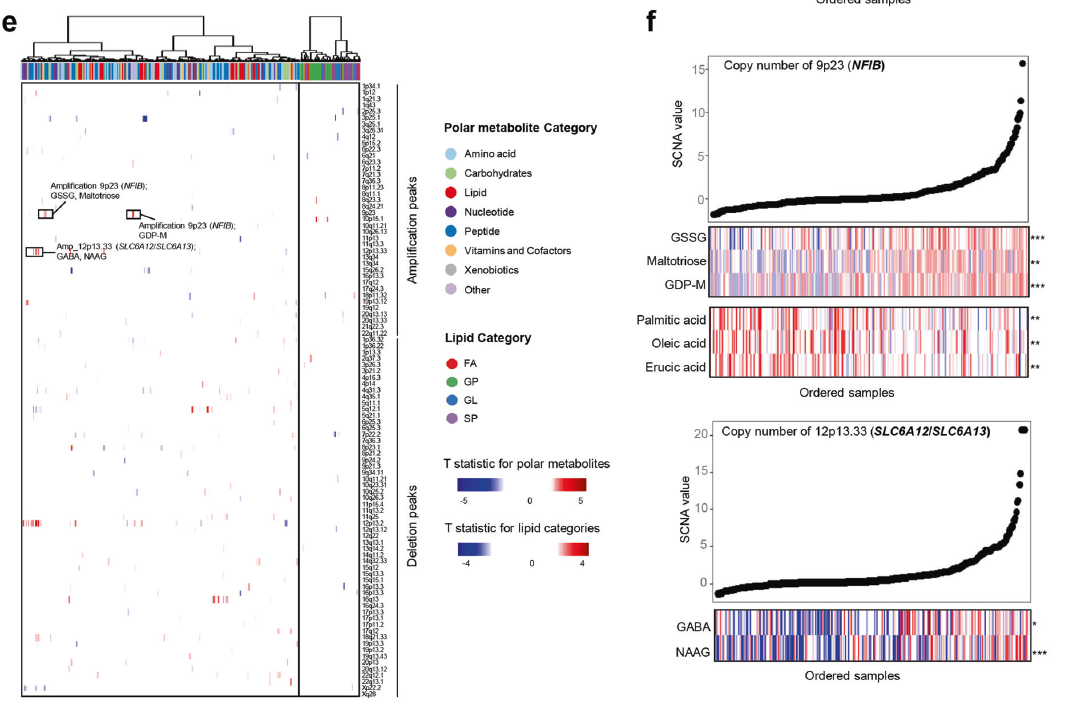
作者還探索了代謝組學和基因組特征之間的聯系,以推測潛在的基因組驅動因素,其如何促進代謝組學特征的形成。最終作者發現了少數代謝物與其配對的代謝基因,如D-甘露糖以及MAN1A1具有顯著相關性,此外作者發現PIK3CA突變與FA豐度正相關,而與GSSG豐度負相關,而BUB1B mRNA表達與s -腺苷蛋氨酸豐度正相關。另外研究表明,染色體12p13.33區域的拷貝數與神經遞質-氨基丁酸(GABA)和n -乙酰天冬氨酸(N-acetyl-aspartyl-glutamate, NAAG)的豐度呈正相關(圖3f)。綜上所述,基因組特征與代謝物相關性的分析可能為研究TNBC代謝重編程的驅動力提供線索。
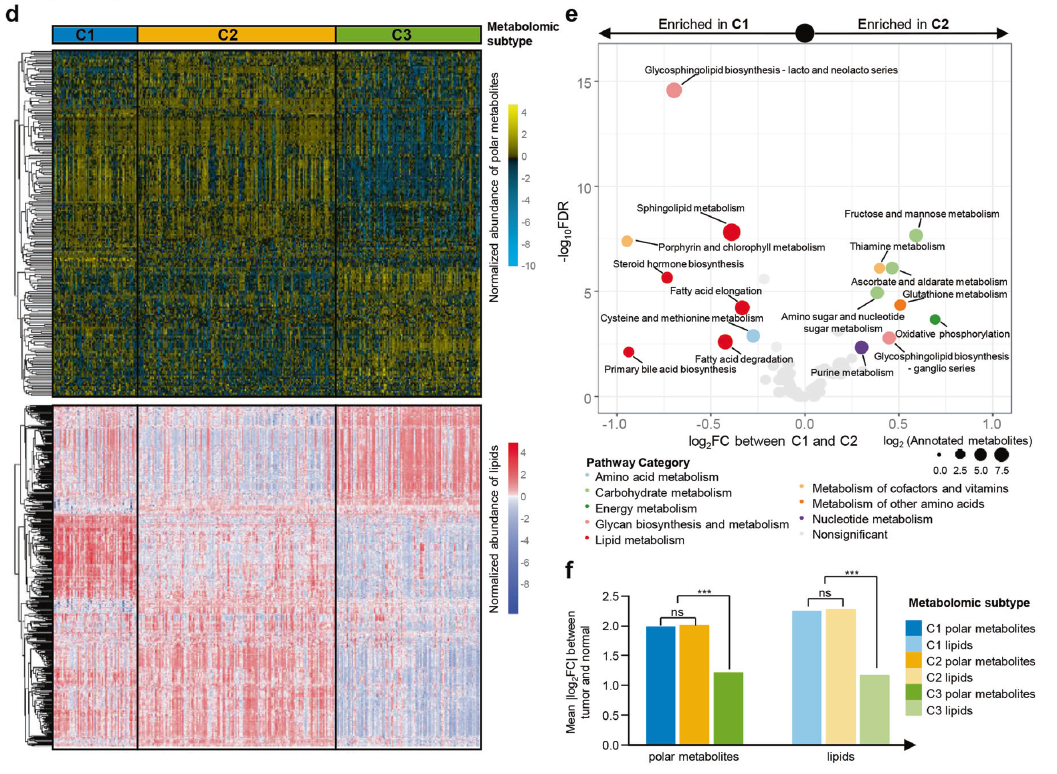
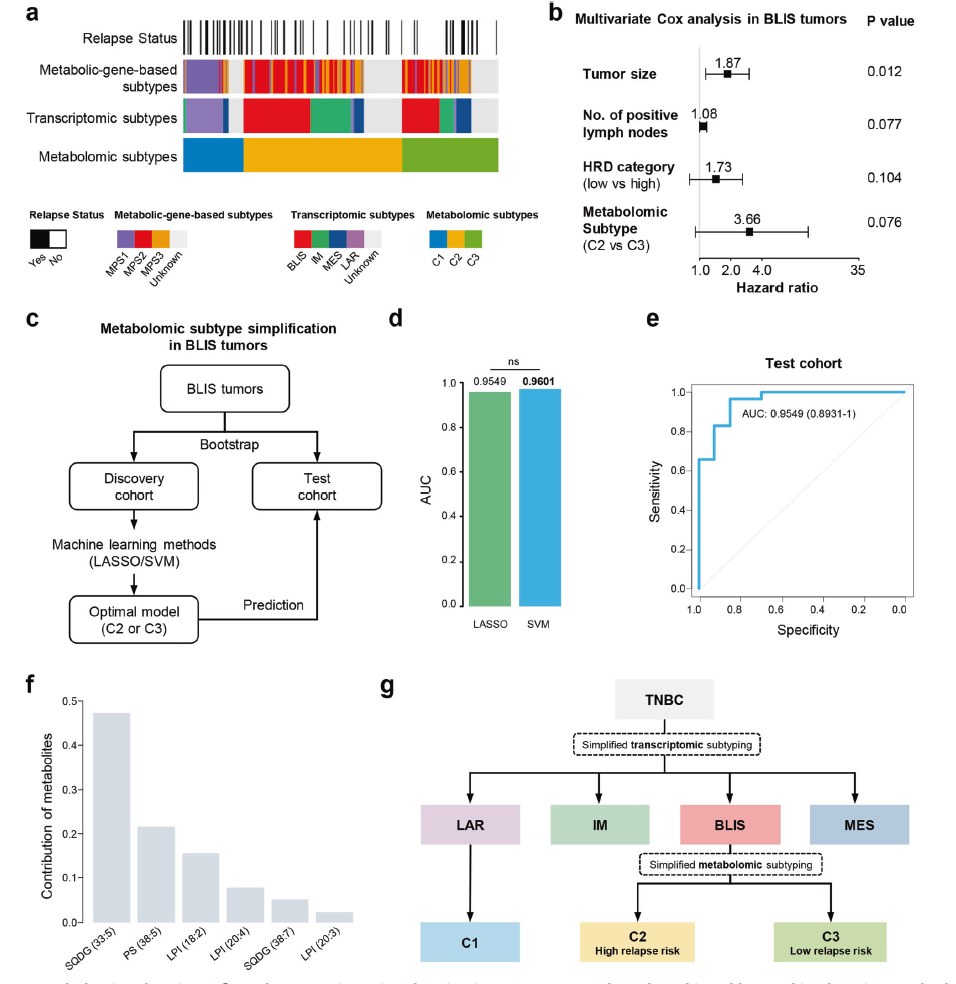
機器學習幫助通過代謝組學實現轉錄組學亞型的細化
作者進一步探討了代謝組學亞型之間的聯系,先前定義的轉錄組亞型4和基于代謝通路的亞型(MPSs)在轉錄組亞型上,LAR亞型幾乎與代謝組C1亞型重疊;BLIS、免疫調節(IM)和間充質樣(MES)亞型主要分為代謝組學C2和C3亞型。總之,代謝組學分析完善了之前研究的TNBC轉錄組亞型。考慮到作者所謂的FUTURE試驗對LAR和BLIS患者的治療效果不理想,代謝組學亞型5分型與轉錄組學亞型分型的整合需要進一步研究。對于LAR腫瘤,可以根據代謝組學C1亞型的特點,進一步探索代謝靶點。對于BLIS患者,簡化的基于機器學習的代謝組學亞型系統可能會將他們劃分為具有明顯復發風險的組。
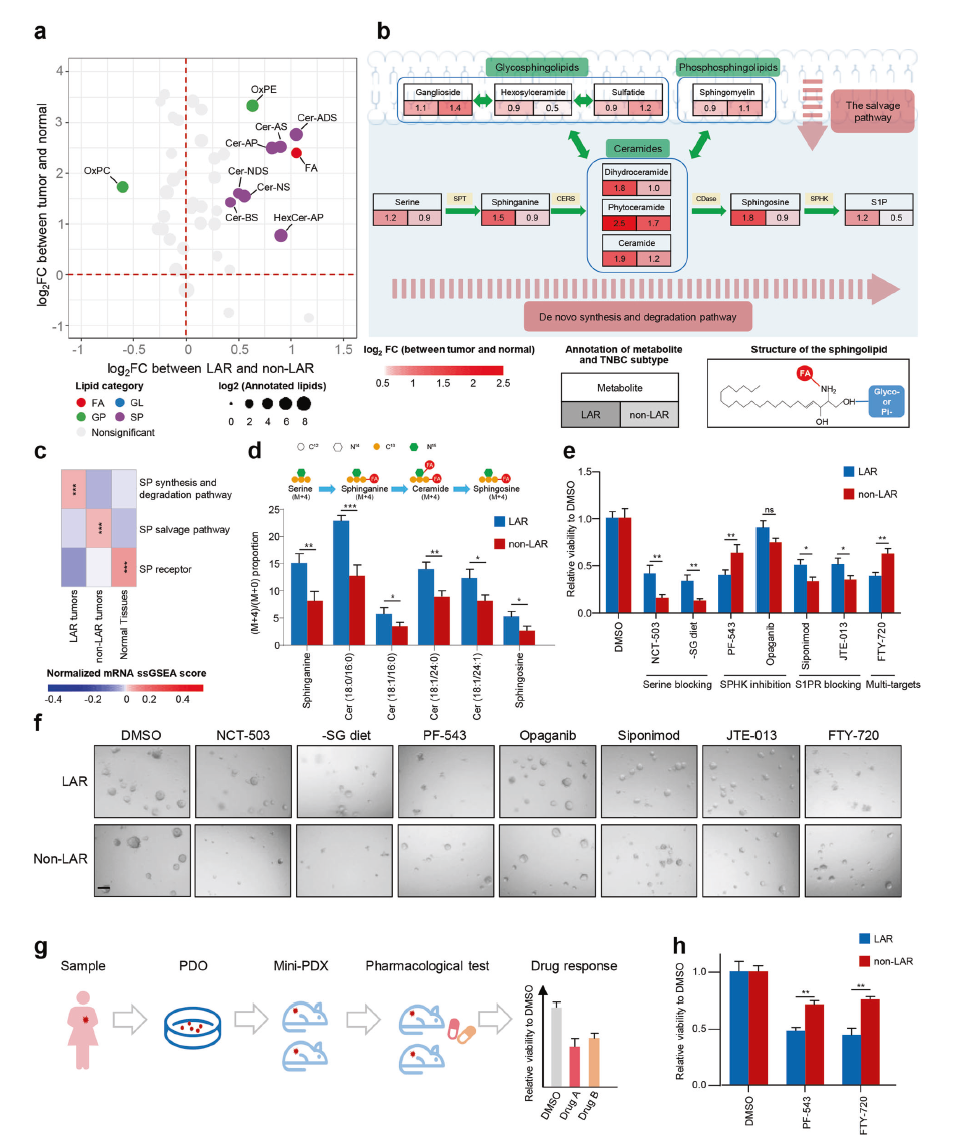
進一步研究發現,神經酰胺途徑的重要中間體S1P在LAR腫瘤中發揮了重要作用。PF-543和FTY-720可能可以特異性治療LAR腫瘤。
NAAG是BLIS腫瘤中重要的促瘤代謝物
作者進一步探索了BLIS腫瘤中重要的促腫瘤代謝物。在分析了在BLIS腫瘤中特異上調且預測預后不良的代謝物后,作者確定NAAG是一個潛在的候選代謝物,通過研究發現NAAG是BLIS腫瘤中重要的促腫瘤代謝物,靶向NAAG的生物合成可能是一種可行的治療BLIS腫瘤的策略。
總結
該研究 成功繪制出當前世界上最大規模的三陰性乳腺癌代謝物圖譜 ,優化了既往分型標準,為三陰性乳腺癌的精準個體化治療提供新方向 ;作為三陰性乳腺癌“復旦分型”研究的延續,研究團隊還針對目前療效最差的兩個三陰性乳腺癌亞型,提出對代謝通路中的關鍵代謝物鞘氨醇-1-磷酸和N-乙酰-天冬-谷氨酸的合成進行抑制,有望成為此類乳腺癌的精準靶向治療的潛在策略。
項目推薦




